科学家首次观察到化学键形成过程 开辟研究新领域
- 来源:互联网
- 作者:唯有花知
- 编辑:ChunTian
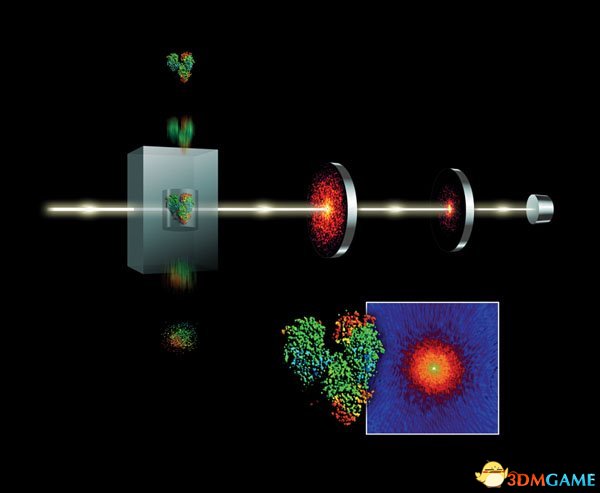
据报道,继2013年科学家通过原子力显微镜看到共价键的结构之后,如今再次直接观察到化学键的形成过程,打破了以往无法观测过渡态化合物的定论。
《科学快讯》(Science Express)刊载了这一研究成果。斯坦福直线加速器中心(SLAC)国家加速实验室的科学家们利用X射线激光观察到了化学反应中形成化学键的过渡状态。由于化学反应中的过渡态化合物的存在时间非常短,直接通过实验方法观测它们在之前很长一段时间内都被认为是不可能的任务。而现在的这一研究成果为化学领域带来了重要的突破。
SLAC实验室及斯坦福表面科学与催化中心(SUNCAT)教授安德斯·尼尔森(Anders Nilsson)是这项研究的领导者。他表示:“这是所有化学领域的核心,我们视之为‘圣杯’,因为它控制着一切化学反应。在化学反应过程中的任何一个时刻,处于这种过渡状态的分子都太少了,所以我们以前一直认为这种现象是无法直接观察到的。”
最终,一种亮度非常高的X射线脉冲打破了这个不可能。这项实验使用了SLAC的直线加速器相干光源(LCLS),这种波长够长,频率也够高的射线脉冲可以捕捉运动中的原子和分子并成像。
研究人员使用LCLS研究了一个发生在固体催化剂表面的反应,类似的反应也发生在汽车的尾气净化器当中:固体催化剂表面“抓取”一氧化碳分子和氧原子并使它们相邻排列,使它们更容易配对生成二氧化碳分子。
在SLAC的试验中,研究人员将一氧化碳与氧原子附着在金属钌为催化剂的表面,并通过一束激光脉冲引发其反应。研究小组通过LCLS的X射线脉冲得以观察到此反应的过程,弄清楚了这些原子周围电子的重新排列情况——这一不易察觉到的微妙过程发生在几飞秒内(飞秒为10-15次方秒)。
“首先氧原子活化,随后不久一氧化碳分子也被激活”,尼尔森说到,“它们开始振动,在约一万亿分之一秒后,它们开始相互碰撞并转变为过渡态化合物。”
研究人员们惊讶于能观察到相当多的进入过渡状态的反应物,同样他们也发现,只有很小的一部分过渡态化合物真正顺利地形成了稳定的二氧化碳分子。剩下的大部分都没能完成反应,而是再次分开成为反应物。


























玩家点评 (0人参与,0条评论)
热门评论
全部评论